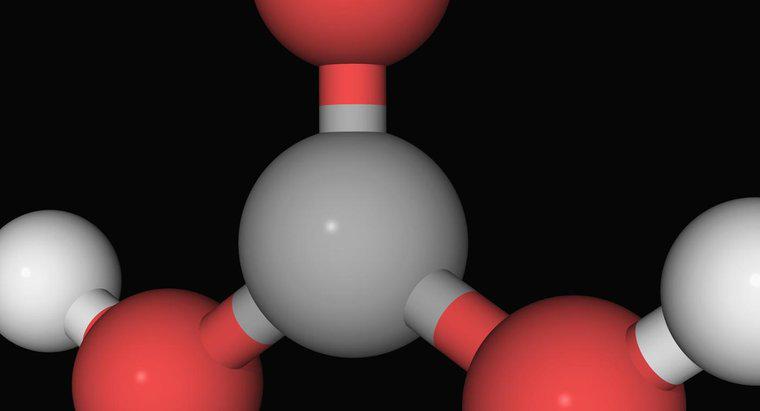
A amônia, um composto gasoso de um átomo de nitrogênio ligado a três átomos de hidrogênio, não é uma base forte. É uma base mais fraca que geralmente deve reagir com a água antes de reagir com um ácido. Antes de neutralizar os ácidos em uma solução, ele reage com a água para formar íons de amônio e hidróxido. O amônio é um íon positivo de um átomo de nitrogênio e quatro átomos de hidrogênio, e é um ácido fraco.
Todas as bases funcionam aceitando íons de hidrogênio, que são apenas prótons nus. Isso neutraliza os ácidos, pois os ácidos atuam liberando íons de hidrogênio para reagir com outros materiais. As bases reagem com esses íons com mais força do que outros materiais e, portanto, podem proteger esses outros materiais dos ácidos. No entanto, as próprias bases podem ser corrosivas.
As bases mais fortes, como o hidróxido de sódio, atuam dissociando seus íons de hidróxido em solução. Os íons hidróxido reagem fortemente com os íons hidrogênio para formar água. Os outros componentes dos ácidos e bases costumam se associar como sais. No entanto, a amônia não contém íons hidróxido. Deve primeiro reagir com água para gerá-los. Isso não apenas adiciona uma etapa antes de neutralizar os ácidos, como também é parcialmente neutralizado pela criação de amônio, um ácido mais fraco.