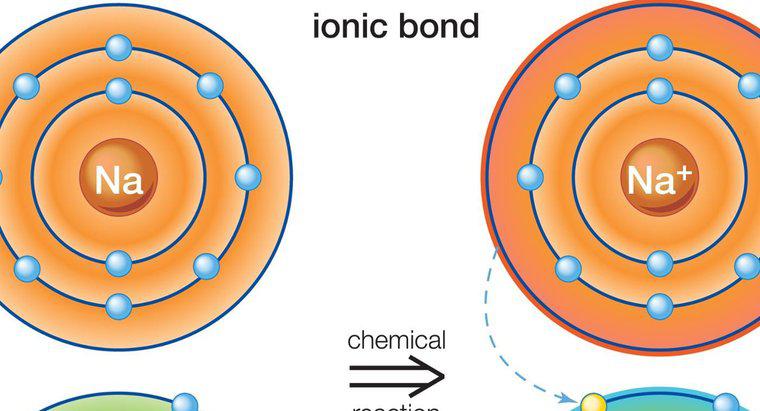
Os compostos iônicos são eletricamente neutros porque as cargas dos cátions e ânions que compõem o composto se cancelam. No caso do sal, por exemplo, o sódio tem uma carga positiva, e o cloreto tem uma carga negativa. Juntos, eles neutralizam o composto.
Os compostos iônicos são constituídos por átomos ou moléculas com carga positiva e negativa. Aqueles com carga positiva são chamados de cátions, enquanto aqueles com carga negativa são chamados de ânions. Os dois são atraídos um pelo outro por causa de suas cargas opostas. Cátions e ânions podem atrair mais de uma molécula do tipo oposto, criando uma molécula mais longa mantida unida por ligações iônicas.
O cloreto de cálcio é outro exemplo de composto iônico, com o cálcio positivo anulando o cloreto negativo. O brometo de ferro faz o mesmo, com a carga positiva do ferro cancelando a carga negativa do brometo. Essa neutralidade elétrica ajuda a manter o composto estável, tornando-o mais fácil de trabalhar e muito menos volátil do que os íons instáveis.
A maioria dos compostos iônicos são sólidos com altos pontos de fusão. Eles geralmente são formados por um elemento metálico e um elemento não metálico. Os compostos que são feitos de dois não metais são frequentemente compostos ligados covalentemente.