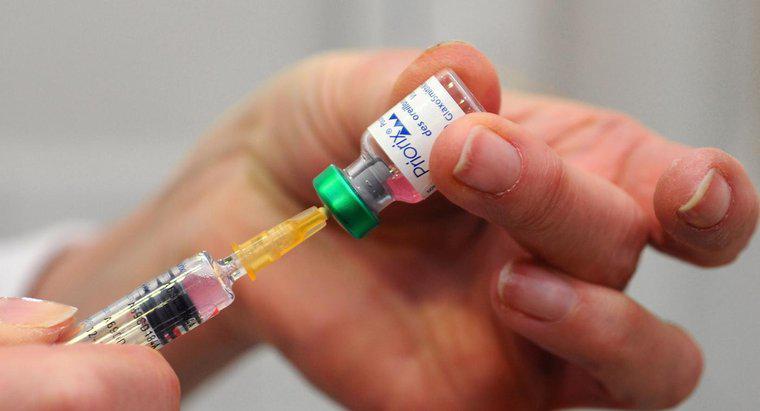
Uma aplicação prática da lei de Boyle é colocar fluido em uma seringa. Puxar o êmbolo aumenta o volume interno da seringa e reduz sua pressão. O fluido fora da seringa é sugado para o cilindro até que as pressões interna e externa estejam equilibradas.
A lei de Boyle afirma que o volume e a pressão de um gás ou líquido permanecem constantes, desde que a temperatura da substância permaneça a mesma. Essa lei, que foi declarada pela primeira vez por Robert Boyle no século 17, é de vital importância em aplicações de engenharia, como design de motores. Sua fórmula é V1 /V2 = P2 /P1 (em temperatura constante), onde V1 é o volume inicial, V2 é o volume modificado, P1 é a pressão inicial e P2 é a pressão modificada.
A lei mais intimamente relacionada à lei de Boyle é a lei de Charles, ou a "lei dos volumes", que é obra do cientista francês Jacques Charles. Ele descreve a relação entre volume e temperatura. Tanto a lei de Boyle quanto a lei de Charles são teorias de gases que descrevem o comportamento de um hipotético gás "ideal". Na prática, entretanto, ambos também se aplicam a líquidos. A lei de Boyle é às vezes chamada de lei de Mariotte, uma referência ao pesquisador francês que descobriu os mesmos princípios 14 anos após a publicação de Boyle. Essa convenção de nomenclatura é popular na França e em outros países europeus.