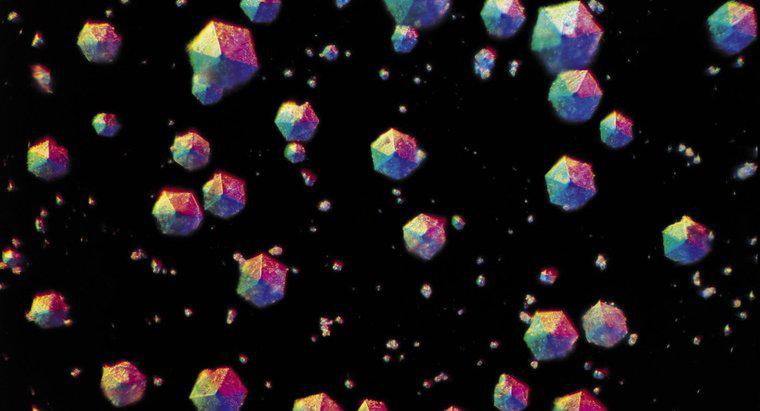A cristalização separa um sólido dissolvido em um líquido que formou uma solução. Para cristalizar o sólido, a solução é aquecida em um recipiente aberto para permitir que o líquido evapore, deixando o sólido cristalino para trás.
A cristalização pode ser induzida natural ou artificialmente. Além dos cristais que precipitam de uma solução líquida, a cristalização também pode ocorrer em um líquido fundido que é resfriado ou em um gás que é depositado em uma superfície. A cristalização ocorre em duas etapas principais: nucleação e crescimento do cristal.
Durante a fase de nucleação, as moléculas de solvente dispersas na solução são atraídas umas pelas outras, formando aglomerados de tamanho nanométrico. Interromper o processo nesta fase e estabilizar os nanoclusters é uma técnica comumente usada na síntese de nanopartículas. Deixar o processo continuar produz núcleos estáveis que persistem sem se dissolverem de volta na solução. O tamanho crítico que esses núcleos precisam atingir para se tornarem estáveis depende das condições do sistema, como a temperatura da solução e a concentração do solvente.
O estágio de crescimento do cristal envolve a atração subsequente de moléculas de solvente adicionais para os núcleos que anteriormente conseguiram atingir o tamanho crítico. Este processo continua enquanto a solução estiver supersaturada: tendo mais solvente dissolvido do que pode sustentar nessas condições particulares.