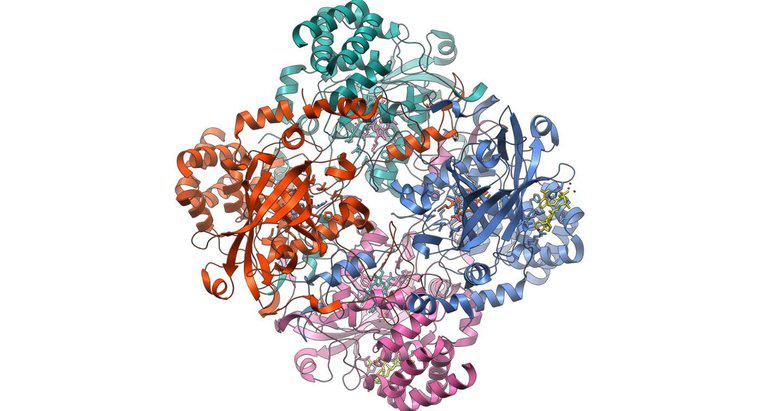
A catalase é uma enzima encontrada em organismos expostos ao oxigênio. Ele decompõe o peróxido de hidrogênio em água e oxigênio, de acordo com a Enciclopédia Britânica. É encontrado em grandes quantidades nos tecidos de mamíferos e ajuda a prevenir danos aos tecidos do peróxido, que é um subproduto de muitas reações metabólicas.
De acordo com o National Institutes of Health, acredita-se que o estresse oxidativo do peróxido de hidrogênio esteja relacionado a muitas doenças crônicas ou de início tardio, como diabetes, asma, Alzheimer e muitos cânceres. De acordo com o Protein Data Bank, a catalase é uma das enzimas mais eficientes encontradas nas células. Uma única molécula de catalase pode quebrar milhões de moléculas de peróxido de hidrogênio. As catalases humanas usam um íon de ferro para ajudar nessa reação muito rápida. Como a catalase está envolvida na quebra de moléculas muito reativas, é incomumente estável para uma enzima. Organismos que dependem de oxigênio para alimentar suas células devem controlar cuidadosamente sua presença em seus sistemas porque o oxigênio é facilmente convertido em outros compostos reativos que podem causar danos significativos. Reações químicas envolvendo elétrons podem converter oxigênio em radicais superóxidos, peróxido de hidrogênio ou radicais hidroxila, todos moléculas perigosas que atacam e mutam o DNA e precisam ser quebradas e neutralizadas.