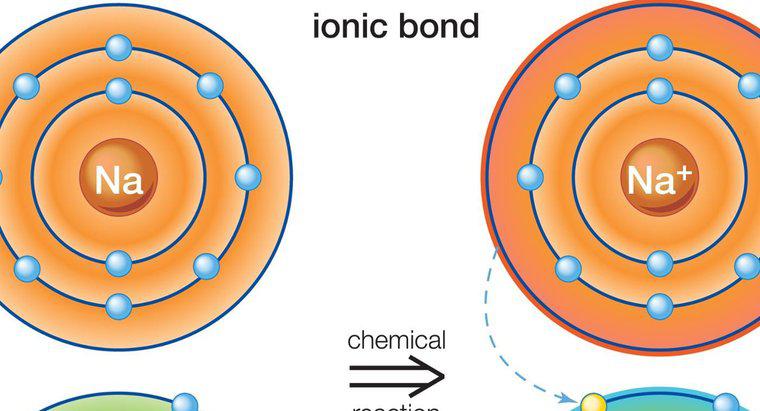
A nomeação de compostos iônicos requer a identificação correta das espécies de cátions e ânions presentes. Em certos casos, a carga do íon é importante para uma nomenclatura precisa.
Os princípios de nomenclatura da química padrão identificam o cátion primeiro no nome e o ânion em segundo lugar. Em compostos iônicos, o cátion é normalmente um metal, e a primeira parte do nome do composto é simplesmente esse metal. Se o cátion pode existir naturalmente em vários estados carregados, a carga do metal, também conhecida como valência, deve ser identificada no nome do composto com algarismos romanos. Por exemplo, o ferro pode existir no estado positivo de duas ou três cargas positivas. Eles seriam chamados de ferro (II) e ferro (III), respectivamente.
A etapa final para nomear um composto iônico é identificar corretamente o ânion que está presente. Os ânions podem ser um único íon, como o brometo, ou moléculas complexas feitas de vários átomos, como o sulfato. Para esses ânions complexos, parâmetros de nomenclatura adicionais estão em vigor. Elementos que são capazes de formar múltiplos oxiânions, como nitrogênio e enxofre, têm uma terminação -ita ou -ato, dependendo do número de moléculas de oxigênio presentes. Um exemplo de um composto iônico adequadamente denominado é o sulfato de ferro (II) para a fórmula iônica Fe (SO4).