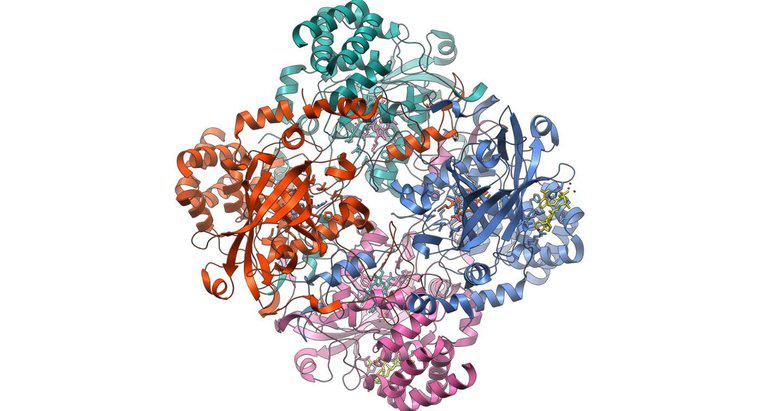
A hemoglobina se liga ao oxigênio enferrujando em nível atômico. A molécula de hemoglobina nas células vermelhas do sangue é o que o Escritório de Ciência do Departamento de Energia dos EUA chama de "metaloproteína". Ou seja, é uma proteína que incorpora algum metal, neste caso o ferro, em sua estrutura. Cada molécula de hemoglobina carrega quatro átomos de ferro ligados que trabalham cooperativamente para transportar oxigênio dos pulmões, onde é abundante, para outras partes do corpo.
De acordo com o site do National Center for Biotechnology Information, os átomos de ferro transportados pela hemoglobina reagem à presença de oxigênio da mesma forma que o ferro costuma fazer, ligando-se a ele em um processo chamado oxidação. O composto resultante, óxido de ferro, é chamado de ferrugem quando é encontrado fora do corpo. Dentro das células vermelhas do sangue, essas moléculas de hemoglobina oxidada retêm sua carga de oxigênio até chegarem a uma parte do corpo que não tem oxigênio suficiente, onde é então liberado.
O mesmo artigo observa que as quatro subunidades da molécula de hemoglobina trabalham juntas para ligar o oxigênio de forma muito eficiente em ambientes ricos em oxigênio, mas o efeito enfraquece em ambientes pobres em oxigênio. Essa reação desigual torna a hemoglobina ansiosa para se ligar ao oxigênio nos pulmões e igualmente ansiosa para se separar dele na presença de uma célula faminta de oxigênio, quando então o ciclo recomeça.