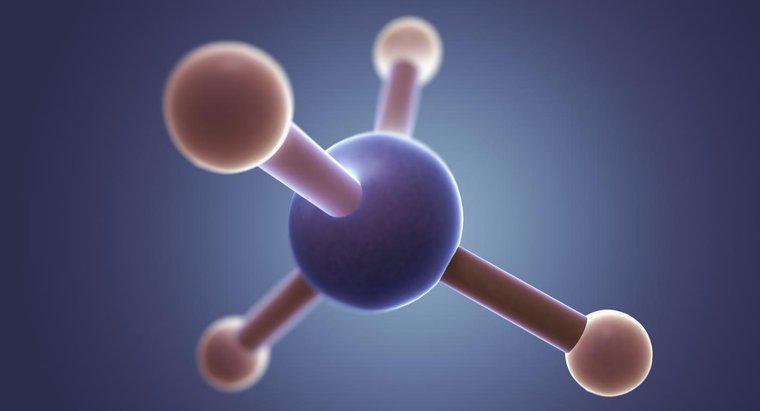
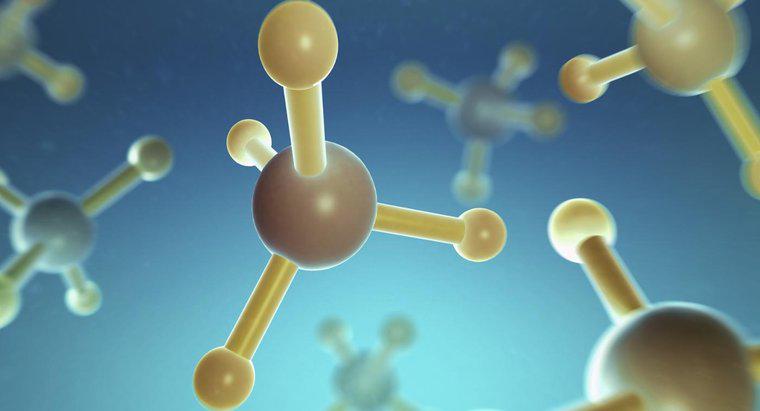
A estrutura da molécula de metano, CH4, exibe ligações covalentes simples. A ligação covalente envolve o compartilhamento de elétrons. Na molécula de metano, os quatro átomos de hidrogênio compartilham um elétron cada com o átomo de carbono.
Algumas propriedades das ligações covalentes são que tendem a ocorrer entre dois átomos não metálicos, têm baixo ponto de ebulição e ponto de fusão e baixa polaridade. À temperatura ambiente, essas moléculas covalentes são gasosas ou líquidas. Por exemplo, o metano é um gás.
Em contraste, as ligações iônicas tendem a estar presentes em compostos sólidos. As ligações iônicas ocorrem entre um metal e um não-metal. Algumas características das ligações iônicas em compostos são que elas exibem altos pontos de fusão e ebulição.